Page 200 - Los elementos químicos: un manual extenso. A. Doadrio
P. 200
Isótopos
Tiene 3 isótopos naturales y estables: Si (92,23%), Si (4,67%) y Si (3,1%) y
28
29
30
18 sintéticos radiactivos.
Estado natural
El silicio prácticamente no se encuentra en estado nativo, lo que es un problema
porque para sus aplicaciones semiconductoras se necesita puro o muy puro. Está presente
en minerales, como óxido: arena, cuarzo, amatista, ágata, pedernal, ópalo y jaspe y en los
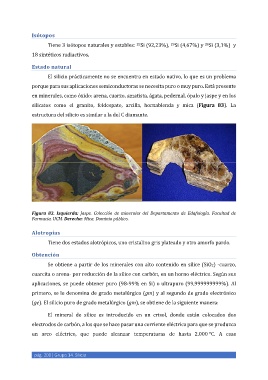
silicatos como el granito, feldespato, arcilla, hornablenda y mica (Figura 83). La
estructura del silicio es similar a la del C diamante.
Figura 83. Izquierda: Jaspe. Colección de minerales del Departamento de Edafología. Facultad de
Farmacia. UCM. Derecha: Mica. Dominio público.
Alotropías
Tiene dos estados alotrópicos, uno cristalino gris plateado y otro amorfo pardo.
Obtención
Se obtiene a partir de los minerales con alto contenido en sílice (SiO2) ‐cuarzo,
cuarcita o arena‐ por reducción de la sílice con carbón, en un horno eléctrico. Según sus
aplicaciones, se puede obtener puro (98‐99% en Si) o ultrapuro (99,999999999%). Al
primero, se le denomina de grado metalúrgico (gm) y al segundo de grado electrónico
(ge). El silicio puro de grado metalúrgico (gm), se obtiene de la siguiente manera:
El mineral de sílice es introducido en un crisol, donde están colocados dos
electrodos de carbón, a los que se hace pasar una corriente eléctrica para que se produzca
un arco eléctrico, que puede alcanzar temperaturas de hasta 2.000 °C. A esas
pág. 200| Grupo 14. Silicio